
Tu Negocio es Nuestro Negocio
RED MERCURY INFORMATIONS - MERCURIO ROJO - MERCURIO SILVER
En abril de 1994 se emitió un documental de televisión, "El Neutrón de Bolsillo", en el que un entrevistado afirmaba que toneladas de una sustancia llamada Mercurio Rojo se contrabandeaban a través de Italia cada año hacia países en desarrollo, lo cual preocupaba gravemente a las autoridades, ya que podría utilizarse en la fabricación de bombas de neutrones. En otra parte del programa se le denominaba óxido de mercurio y antimonio y, más acertadamente, sal de mercurio del ácido antimónico, lo que, dada su fórmula, parecería indicar ácido piroantimónico en lugar de metaantimónico. En consonancia con un programa anterior sobre este tema, también se le asignó el nombre en clave de este óxido doble, RM 20-20, y se atribuyó su producción al progreso científico ruso, a la vez que se repetía la afirmación del Ministerio de Defensa de que era inexistente.
Al parecer, el mecanismo de funcionamiento del RM 20-20 en las bombas de neutrones es que refleja la radiación neutrónica, una cualidad que se aprovecha al utilizarlo como material de embalaje para plutonio o tritio (1 kg). Supuestamente estaba presente en cada ojiva de los misiles SS-20. Su efecto, al usarse junto con el gas tritio, por ejemplo, era generar fusión termonuclear mediante la producción de grandes concentraciones de energía nuclear. Una estimación en el programa anterior, "La Caza del Mercurio Rojo", indicaba que solo se necesitaría una taza de material fisible en RM 20-20 para destruir Manhattan. Testigos rusos describieron el proceso como lento y difícil. Un especialista militar, entrevistado por el físico estadounidense Dr. Frank Barnaby, mostró una muestra de "Mercurio Rojo líquido", pero se negó a dar detalles sobre su fabricación. Un científico ruso, anteriormente empleado en el estamento militar, fue más directo y, durante la entrevista, el Dr. Barnaby dibujó una estructura química:
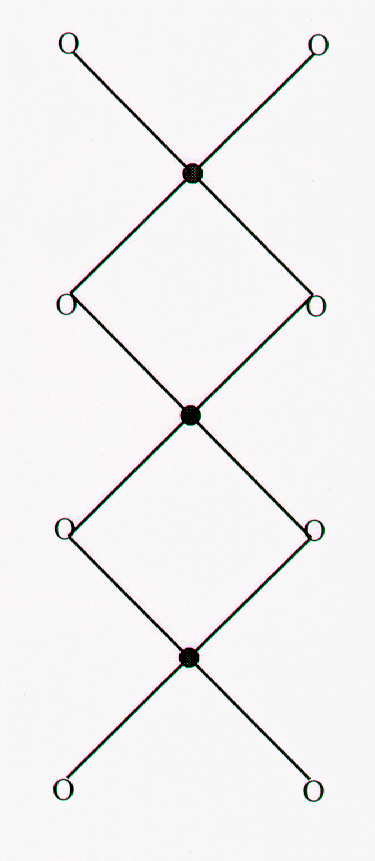
Sin embargo, los realizadores del programa "Dispatches" se sintieron incapaces de transmitir el diálogo de esta entrevista. De vuelta en Estados Unidos, el Dr. Sam Cohen, en gran medida responsable del desarrollo de la bomba de neutrones en la década de 1950, ofreció su evaluación del progreso ruso hacia una bomba de fusión nuclear de bolsillo. En aquel momento, estaba más preocupado que en casi cualquier otra ocasión anterior, afirmó, y la raíz de su preocupación era la existencia del RM 20-20.
Al intentar descubrir la estructura del compuesto y, por lo tanto, evaluar la probabilidad de su existencia y los requisitos para su producción, surgen dos opciones. La primera consiste en examinar compuestos con características o componentes similares y buscar evidencia documental de su síntesis. El Dr. Arthur Sleight elaboró un informe que describe su síntesis y estructura, llevado a cabo en Estados Unidos en 1968, mientras que se afirma que el Dr. Oleg Sadykov lo descubrió ese mismo año, en la antigua URSS. La idea de que estos dos eventos no estuvieran relacionados es, por supuesto, ridícula. La segunda opción consiste en consultar e investigar los esfuerzos de quienes intentaron promover la transformación nuclear del plomo y el mercurio mediante la aplicación de un polvo notablemente similar al utilizado en la producción de RM 20-20: los alquimistas. La asociación del mercurio y el antimonio entre sí y con el elemento objetivo de los alquimistas, el oro, está lejos de ser la única razón para creer que los eligieron para la creación de su polvo transmutador, la llamada Piedra Filosofal. Las referencias en su literatura a «Nuestro Plomo» (antimonio) y las afirmaciones de que sus prescripciones de no usar mercurio común eran meras palabras ambiguas son demasiado prominentes como para ignorarlas. Cabe destacar que el polvo y el RM 20-20 no son lo mismo, pues los creadores de los dos programas «Despachos» fueron engañados. El polvo debe ser «proyectado sobre» (amalgamado con) mercurio para lograr su «multiplicación», en terminología alquímica, seguido de la adición de una pequeña cantidad de actínido y la compresión en el núcleo de un reactor de 4 MW hasta que se produce el agente de empaquetamiento viscoso, el «Mercurio Rojo». Este ejemplo ilustra cómo un área de estudio puede servir para iluminar otra.
Los experimentos para producir el polvo deben comenzar con los reactivos más comunes y progresar a la variedad menos estable utilizada por el Dr. Sleight hasta lograr el éxito. Por mi parte, esto implicó probar una combinación de sulfuros de antimonio y óxidos de antimonio y mercurio para averiguar si estos reaccionarían de tal manera que desplazaran los iones de sulfuro, formando el óxido doble, siendo la sustitución de sulfuros por óxidos una característica común de la producción minera subterránea; los resultados se denominan productos de alteración. Luego tomé el compuesto estable restante, agregué óxido de mercurio (HgO) de nuevo y mariné el resultado en una solución de peróxido de sodio. Después, le agregué cloruro de mercurio (HgCl₂ ) , calentándolo en cada etapa del proceso y anotando cualquier cambio. Finalmente, lo calenté a unos 400 ° C para averiguar qué parte se mantendría estable.
Una breve descripción del compuesto y compuestos relacionados, con sus formas cristalinas básicas.
Piroantimoniato mercúrico Hg2Sb2O7
MP 356.6 0 C
Color: Rojo cereza
Densidad: 9,02 g/cc o 9,6 g/cc
Estructura: Por analogía con el K 2 Cr 2 O 7 , monoclínico/triclínico, o, utilizando HgSb 2 O 6 e IF 7 como estructuras iónicas básicas, un desarrollo del tipo bipiramidal pentagonal u octaédrico.
Producción : Hipotéticamente, al desplazar el ion H + en H4Sb2O7 , se obtiene ácido piroantimónico, pero la reacción esencial sería:
2HgO + Sb 2 O 5 ---> Hg 2 Sb 2 O 7
A 200 ° C el ácido piroantimónico se convierte en ácido metaantimónico y, a 300 ° C, en pentóxido de antimonio, proceso que podría facilitar la reacción:
![]() (2) 2HgO + H 4 Sb 2 O 7 → Hg 2 Sb 2 O 7 + H 2 O
(2) 2HgO + H 4 Sb 2 O 7 → Hg 2 Sb 2 O 7 + H 2 O
También puede valer la pena tener en cuenta el hecho de que la mayoría de los antimoniatos contienen el ion [Sb(OH) 6 ] - , que deriva del pentóxido.
El compuesto más cercano en términos de valencia al piroantimoniato es el que contiene el elemento clave del Grupo 5, el fósforo, a saber, el pirofosfato de mercurio, Hg 2 P 2 O 7 , que forma un sistema acuoso Hg 2 2+ - P 2 O 7 4- pero hay mucha menos documentación para él que para el ortofosfato Hg 3 (PO 4 ) 2 . El metaantimoniato, HgSb 2 O 6 , por el contrario, está entre los pocos óxidos de mercurio mixtos sólidos que se han investigado estructuralmente. Forma cristales hexagonales, isomorfos con PbSb 2 O 6 , en los que las capas de octaedros de SbO 6 enlazados están separadas por capas de Hg. Sugiriendo como lo hace que el piroantimoniato debería tener la fórmula estructural Hg 2 O.Sb 2 O 6, claramente hay otra analogía para ello que involucra la configuración de las unidades iónicas de óxido mercurioso, siendo estas Hg 6 Cl 4 O. Este está estructurado con moléculas de Hg 2 Cl 2 ligeramente deformadas conectadas a través de los aniones Cl - a cadenas infinitas de Hg 2 O.
Compuestos posiblemente análogos al piroantimoniato mercúrico en estructura iónica y forma cristalina:
Mg 2 P 2 O 7 , K 2 Cr 2 O 7 , Mn 2 P 2 O 7 , Ca 3 (PO 4 ) 2 , Hg 2 CrO 4 , HgCrO 4 , HgSb 2 O 6 , K 4 P 2 O 7 , K 2 H 2 Sb 2 O 7 , M 2+ Sb 2 O 6 , (M = Mg, Fe, Co , Ni , Zn ) , MnSb2O6 , Ca2P2O7 .
Mg₂P₂O₄ : tabletas monoclínicas. K₂Cr₂O₄ : rojo, mono/triclínico. Mn₂P₂O₄ : monoclínico . Ca₃(PO₃) ₂ : escoria fusible . Hg₂CrO₃ : agujas / polvo rojo . + HgCrO₃ : rojo , rómbico / ortorrómbico . HgSb₂O₄ : trirutilo . M₂ + Sb₂O₄ : trirutilo. MnSb₂O₄ : columbita octaédrica . Ca₂P₂O₄ : monoclínico ( alfa ) , tetragonal / uniaxial , cristales positivos ( beta ) .


Sulfuros y óxidos mercúricos y antimónicos como minerales
El mercurio y el antimonio se encuentran en varios lugares del mundo, especialmente en España, México, Rusia y China, en forma de sus sulfuros minerales, cinabrio y estibina. El cinabrio es sulfuro mercúrico, la estibina es sulfuro de antimonio. En raras ocasiones, estos dos pueden unirse para formar un solo mineral, como en el caso de la livingstonita, Hg Sb 4 S 8 . Aunque de color gris acero, deja una veta roja cuando se frota contra la piedra de toque, y finas láminas de la roca presentan una translucidez rojiza cuando se sostienen a contraluz. Su forma cristalina es monoclínica, tiene una densidad de 4,9 g/cc y se encuentra asociado con el cinabrio, la estibina y la valentinita. Se ha informado de que entre los lugares de su aparición se incluyen Chaidarkan en la antigua URSS y México.Los óxidos minerales de mercurio y antimonio existen como productos de alteración de sus sulfuros. Los productos de alteración se forman debido a la exposición de los minerales fuente al vapor y al gas que emiten los respiraderos en las formaciones rocosas circundantes en un proceso que puede durar milenios. Como resultado, son mucho más raros que sus sulfuros. La valentinita es una forma de trióxido de antimonio (Sb2O3 ) y tiene una forma cristalina rómbica ; la senarmonita, que tiene una forma cúbica, es otra. Por lo tanto , se dice que el trióxido de antimonio es dimorfo. El óxido mercúrico, HgO, existe en la naturaleza en su forma mineral montroydita. Esta es de color rojo oscuro a marrón, con una translucidez vítrea, pero puede ser transparente en secciones suficientemente delgadas. Sin embargo, deja una veta marrón amarillenta en la piedra de toque. Tiene un sistema cristalino ortorrómbico y una densidad de 11,2 g/cc. No es sorprendente que se encuentre asociado con mercurio, cinabrio y/o calomelanos (cloruro de mercurio) en cinco lugares de California y uno de Texas.
A veces , la exposición tanto al oxígeno como al vapor producirá un compuesto doble que comprende óxido e hidróxido, como en el caso de la estibiconita, u óxido de antimonio hidratado, Sb3O6 ( OH ). En su forma pura, este es blanco tiza, pero tiene una gama de otros colores, amarillo pálido o más oscuro en tono, asociados con diferentes impurezas. En láminas finas es translúcido a transparente. Tiene un sistema cristalino cúbico y una densidad que varía de 3,3 a 5,5 gm/cc. Ocasionalmente se puede encontrar en grandes agregados de cristales que reemplazan a la estibina con la que normalmente se asocia, pero más comúnmente con el óxido puro, valentinita. Se encuentra en muchos más lugares que la montroydita, estando ampliamente presente en el oeste de EE. UU. y México, también en Bolivia, Perú, Inglaterra, España, Italia, Rumania, Argelia, Borneo, Australia y China.
La oxidación incompleta de la estibina puede producir kermesita, la forma mineralizada del oxisulfuro de antimonio, 8[Sb₂S₂O ] . Sus cristales rojos, aciculares, contienen formas cristalinas monoclínicas y ortorrómbicas , y se presenta asociada a la valentinita y la senarmonita. Obsérvese la densidad mucho mayor del óxido de mercurio en relación con la livingstonita. Esto contradice las expectativas basadas en las altas densidades del antimonio (6,69 g/cc) y el azufre (2,07 g/cc) en relación con la densidad del oxígeno (1,33 g/cc), pero se debe a los enlaces electrónicos adicionales asociados con la presencia de los iones de un tercer elemento. Estos ocupan el espacio que, de otro modo, estaría ocupado por los iones del compuesto simple de dos elementos y poseen una masa insignificante. Por lo tanto, los compuestos dobles o ternarios tienen una densidad menor que los compuestos simples que comprenden elementos similares. Esto representa una consideración importante en relación con la densidad máxima posible de una amalgama que contiene piroantimoniato mercúrico, cuya densidad medida es de 9,02 g/cc (véase la Parte II). Cabe destacar también la prevalencia de formas cristalinas cúbicas y rómbicas entre los óxidos, lo cual constituye una pista útil para la forma cristalina de dicho óxido ternario.El polvo de mercurio rojo, suponiendo que se descubrió originalmente en el suelo en lugar de sintetizarse (una suposición respaldada por las dificultades de su producción), parecería ser uno de estos productos de alteración y haberse generado únicamente donde tanto el cinabrio como la estibina se oxidaban muy cerca. Debido a la alta prevalencia de depósitos de cinabrio que se encuentran junto con la estibina en toda China central, parece probable que el mito/relato de la Piedra Filosofal tenga su origen en ese país, siempre que comparta una identidad común con el piroantimoniato mercúrico o alguna variante estrechamente relacionada de este óxido ternario. Por otro lado, para un caso específico de asociación mineral entre los componentes del mercurio rojo y Rusia, puede consultarse la entrada del Chemical Abstract Services en el volumen 125 (1996) «Contenido de mercurio y antimonio en los minerales del depósito de Hg-Sb de Nikitovka», Rusia 280881n.
SOBRE LAS ESTRUCTURAS IÓNICAS O MINERALES QUE PUEDEN INFLUIR EN LA NATURALEZA DEL COMPUESTO BASE DEL MERCURIO ROJO.
El dicromato de potasio, al ser un compuesto común y estable con una estructura similar a la del compuesto supuestamente inestable, el ácido piroantimónico, parecería ser un buen punto de partida para determinar la estereoquímica del piroantimoniato de mercurio, particularmente al decidir dónde colocar los iones de mercurio.Al igual que el ion hidróxido de antimonio, el ácido piroantimónico se asocia con el óxido ácido, pentóxido de antimonio, cuya estructura es ditetraédrica (véanse los diagramas 1 y 2). La posición de los iones potasio en el dicromato proporciona una idea inicial de cómo los iones mercurio podrían unirse al ácido deshidrogenado (véase el diagrama 2).
Entretanto, dado que la Piedra era considerada como producto de componentes naturales, como la "quintaesencia", el "vapor húmedo" que, al pasar a través de los estratos geológicos, hacía que los metales se reprodujeran bajo tierra, parecería apropiado que se examinaran los minerales que probablemente se utilizaron en la Obra.
La estibiconita, u óxido de antimonio hidratado (Sb₂O₆ ( OH )), es un mineral amarillo, blanco en estado puro, con una forma cristalina prismática. La kermesita (2Sb₂O₆.Sb₂O₃ u 8 [ Sb₂S₂O ] ) es un polvo grueso de color rojo oscuro, que se vuelve negro al calentarse , pero vuelve a rojo al enfriarse, y forma agregados de cristales ligeros y plumosos si hay un poco de agua de cristalización. El cinabrio (HgS) es igualmente rojo y forma cristales hexagonales, la misma formación que adopta el HgO naranja (véanse las fotos de los agregados cristalinos). Si estas estructuras minerales estuvieran muy próximas, no sería sorprendente que, una vez vaporizado el azufre, dieran lugar a un producto de alteración, un óxido doble simétrico a pesar del número impar de iones que poseía en cada unidad de fórmula
LA DISTINCIÓN ENTRE COMPUESTOS ORTO-, META- Y PIRO-.
Estos prefijos se utilizan para indicar los niveles relativos de oxidación en óxidos dobles, aquellos que contienen dos metales o un metal e hidrógeno. Los compuestos orto son simplemente compuestos ordinarios, como lo sugiere el prefijo, que se asocia con la descripción de algo como "adecuado", "normal" o "correcto", por ejemplo, "ortodoxia", que significa "la doctrina estándar". Por lo tanto, los ortofosfatos, por ejemplo, se denominan simplemente fosfatos. Los compuestos piro, como sugiere el prefijo, implican oxidación por acción del calor. El ácido pirofosfórico se forma rápidamente, en forma de cristales granulares blancos, cuando el ácido ortofosfórico se calienta por encima de 240 ° C.
1 ) 2H3PO4 → H4P2O7 + H2O
Los compuestos meta representan un nivel intermedio de oxidación entre los óxidos orto y piro. El ácido metafosfórico se forma a partir del ácido ortofosfórico al calentarse a 316 ° C:
2 ) 2H3PO4 →HPO3 + H2O
Obsérvese que al duplicar el número de moléculas interactuantes involucradas para compararlas con las del caso anterior y equilibrar la ecuación se obtiene una fórmula empírica para el ácido metafosfórico de 2(HPO 3 ) o H 2 P 2 O 6 . La secuencia de iones óxido O 3 , O 6 y O 7 correspondiente a los niveles de oxidación orto, meta y piro resulta ser bastante estándar para diferentes compuestos. El ácido ortoantimónico es H 3 SbO 4 , el ácido metaantimónico HSbO 3 (empíricamente equivalente a H 2 Sb 2 O 6 ) y el ácido piroantimónico H 4 Sb 2 O 7 . Independientemente de los argumentos desarrollados durante los últimos 50 años en el sentido de que estos pueden ser "realmente" hidróxidos, la experiencia de su naturaleza muestra que son fuertemente ácidos.
Sustituyendo mercurio por hidrógeno en la ecuación 1) y ajustando la diferencia de valencia se obtiene:
3) 2Hg 3 (PO 4 ) 2 → 2Hg 2 P 2 O 7 + O 2
y esta es la reacción observada. Sin embargo, aunque podría suponerse que los equivalentes de antimonito para estos fosfatos serían prácticamente alcanzables, este no parece ser el caso. Se sabe que existe el tetróxido Sb 2 O 4 , que se obtiene del calentamiento del trióxido Sb 2 O 3 , y el antimonito de potasio, K 3 SbO 4 , junto con el piroantimoniato de potasio ácido, K 2 H 2 Sb 2 O 7 , 6H 2 O, se han obtenido de manera similar (Textbook of Inorganic Chemistry: JR Partington (1931)), la sustitución de mercurio por potasio en estos compuestos no representa ninguna reacción que haya podido obtener. ya sea en mi investigación sobre experimentos reportados o por mi propia cuenta.
El piroantimoniato de plomo se describe en los siguientes términos en 'Introducción a la química inorgánica avanzada' de Durrant & Durrant:
El piroantimoniato es un polvo amarillo oscuro con una densidad de 6,72 g/cc. Es insoluble en agua fría o caliente, y muy poco soluble en ácido clorhídrico. El compuesto se encuentra en la naturaleza como el mineral bindheimita. Tiene una estructura cúbica. Los cristales tienen una estructura de piroclorito con borde celular, a = 10,47 A.
En las estructuras de piroclorito, los grupos octaédricos SbO₃ comparten cada oxígeno (ion) con otro grupo, de modo que la composición reticular es SbO₃ ( véase el diagrama 4). Aunque el séptimo oxígeno (ion) no es esencial para la estabilidad reticular, hay espacio para él.
Esta consideración cobra especial relevancia al considerar la estabilidad del Hg₂Sb₂O₄ . Es difícil acomodar números impares de átomos de cualquier elemento en estructuras simétricas, ya que estas estructuras , especialmente las cúbicas, presentan la mayor estabilidad gracias a su simetría cuádruple. Si la pérdida del séptimo ion produjera un compuesto más estable, la descomposición de piroantimoniato a metaantimoniato debería ocurrir pronto.
'Preparación.
El piroantimoniato de plomo se puede preparar calentando mezclas de nitrato o acetato de plomo con ácido antimónico, H₃SbO₃ , al rojo vivo. Durante el enfriamiento lento en un horno de refinación de plomo , se forma un óxido de Pb-Sb idiomórfico ( es decir , de una forma peculiar de ese compuesto), muy similar a la bindheimita cúbica , Pb₂Sb₂O₃ .
Aplicaciones.
El amarillo de Nápoles es una mezcla de antimonitos y antimonatos de plomo que se utiliza como pigmento en cerámica y pinturas al óleo (por lo que me resulta de especial interés). La adición de antimonato de plomo al titanato de plomo modifica sus propiedades ferroeléctricas.
El pirofosfato mercúrico, Hg₂P₂O₃ , también ha encontrado aplicación práctica en la fabricación de lámparas eléctricas y tubos electrónicos que contienen vapor de Hg. Según un informe de la Compagnie Générale de Telegraphie sans Fil, 1964-65 .
Se describe el uso de pirofosfato de Hg como sustancia generadora de Hg, en lugar de Hg elemental, para llenar tubos de vapor de Hg con la cantidad exacta de Hg necesaria para su perfecto funcionamiento. La aplicabilidad del Hg₂P₂O₄ para este propósito se basa en su alta estabilidad térmica hasta 600 ° C y su descomposición cuantitativa entre 600 y 800 ° C. Estas propiedades garantizan que no se pierda Hg durante la desgasificación y que se cargue en los tubos exactamente la cantidad teórica de Hg durante el llenado del proceso de fabricación.
UNA CONCLUSIÓN SOBRE LA ESTRUCTURA DEL PIROANTIMONATO DE MERCÚRICO
El Hg2Sb2O7 tiene una estructura cristalina OCTAHÉDRICA .( Ref . Wells : Química inorgánica estructural.):-
La química del oxígeno del antimonio pentavalente era antiguamente muy compleja, y muchos compuestos se describían como orto-, meta- y piroantimoniatos, con fórmulas análogas a las de los fosfatos. El estudio de las estructuras de muchos de estos compuestos cristalinos ha revelado que su química estructural es muy simple y muy diferente a la de los fosfatos, arseniatos y vanadatos, basándose no en la coordinación tetraédrica, sino en la octaédrica, del Sb(V) por el oxígeno... ya sea como iones Sb(OH) ₆ en compuestos que antes se describían como meta- o piroantimoniatos hidratados, o como grupos SbO₆ en compuestos de los siguientes tipos: SbO₃ , M(III)SbO₃ , M(II)Sb₂O₃ , M₂ ( II ) Sb₂O₃ ( subrayado mío ) .
Además, el metaantimoniato de mercurio tiene la misma estructura cristalina que el trirutilo Pb(ll)Sb₂O₃ . El Pb₂Sb₂O₃ tiene una estructura de piroclorito . En estas estructuras, los grupos octaédricos SbO₂ comparten cada oxígeno con otro grupo, de modo que la composición reticular es SbO₃ . Esto genera octaedros con iones de óxido en cada vértice compartido.
Un experimento para determinar la propensión del mercurio y el antimonio a formar óxidos mixtos.
PRUEBA 1. Tras tostar la estibina, fundir el antimonio impuro (Sb) derivado y combinar un poco del compuesto cristalino enfriado con HgO, se observó que el Hg se evaporaba de la mezcla; una reacción típica. Sin embargo, quedó un compuesto rojo oscuro que resistió el calentamiento a 400 ° C, tornándose negro y ligeramente líquido, retornando al rojo al enfriarse. Se añadió un poco de agua y cristalizaron formas finas, como agujas, en su superficie. Al añadir una pizca de esto a un poco de HgO y agua, se desarrolló una reacción exotérmica una vez que la mezcla se calentó moderadamente. La repetición cuidadosa del proceso condujo, una vez más, a la separación del Hg de los demás constituyentes y a su posterior separación en compuestos de antimonio.
Observaciones e interpretación.
Inicialmente, una pequeña parte de la mezcla gris-rosada producida tras la segunda operación resultó ser soluble. Al calentarse, se tornó marrón, pero al enfriarse, se separó en un precipitado gris debajo de una solución marrón-anaranjada. Esta se tornó rojiza al recalentarse, pero finalmente se enfrió, dando lugar a una fina capa roja que precipitó sobre una gris clara. Los efectos de este proceso son prácticamente los mismos que cuando los compuestos constituyentes se calientan por separado, lo que ilustra la constante dificultad de lograr la unión de estos metales resistentes. Las ecuaciones de reacción obtenidas aquí parecen ser:
2HgO → 2Hg + O2
y Sb 2 S 3 .Sb 2 O 3 (aq) → Sb 2 S 3 (s) + Sb 2 O 3
(¿Kermesita?) calentado
La situación es un tanto extraña ya que, aparentemente, la presencia de antimonio en el cinabrio no es infrecuente y dificulta la refinación del mercurio, lo que sugiere una amalgamación de los metales; pero las amalgamas de HgSb no parecen estar enumeradas.
PRUEBA 2. Esta prueba está diseñada para comprobar la similitud del comportamiento del Hg y el Sb en presencia de un metal alcalino con el del Mg y el P combinados con NH₃ . Si se forma un solo compuesto, este podría descomponerse posteriormente según la ecuación de reacción:
2 Mg(NH 4 )PO 4 → Mg 2 P 2 O 7 + 2NH 3 + H 2 O
Por analogía, 2 HgNaSbO 4 → Hg 2 Sb 2 O 7 + Na 2 O
21
Se añadieron antimonio, su trióxido, su pentóxido y su trisulfuro al HgO hasta obtener aproximadamente 2 g de la mezcla. Se calentó en un matraz de fondo plano de 150 ml con un tubo de escape curvado hasta que se produjo una reacción exotérmica. Tras dejar enfriar, se trasladó a una cápsula de evaporación y se calentó hasta que, debido a su aspecto uniforme, se identificó como un solo compuesto. Se añadió solución de peróxido de sodio a una muestra, junto con un poco de kermesita (?) de la Prueba 1, y se dejó en remojo durante la noche. Posteriormente, se calentó hasta que se observó la formación de otro compuesto térmicamente estable.
Observaciones e interpretación.
Inicialmente marrón oscuro, la mezcla se volvió negra al calentarla. La reacción exotérmica se desarrolló vigorosamente; una prueba de astillado confirmó la emisión de oxígeno gaseoso, con condensación de vapor gris claro y blanco en el interior del matraz. La mezcla se tornó gris claro, luego rojiza al enfriarse, formándose un efecto espejo en el interior del matraz. Al cristalizar, apareció una costra pálida y pulverulenta sobre los cristales rojo claro. La adición de agua restauró el color marrón, pero al recalentar el producto apareció un color rojizo, acompañado de un efecto textural similar al de la arcilla. Mientras tanto, la aparición de pequeñas perlas de Hg en su superficie indicó que aún no se había logrado un compuesto estable. Al añadir peróxido de sodio y kermesita (?), se observó la formación de una solución ámbar opaca que luego se aclaró, dejando un precipitado rosado. Al calentar, el Hg reapareció gradualmente en forma de pequeñas perlas sobre el precipitado. Cabe suponer que, en un primer momento, la reacción:
Sb + Sb 2 O 3 + Sb 2 S 3 + 2HgO → Sb + 2Sb 2 O 3 (v) + Sb 2 S 3 (v) + 2Hg(v) + 2O 2
ocurrió, y posteriormente: -
2Sb 2 S 3 + Sb 2 O 3 + Sb 2 S 3 . Sb 2 O 3 (acuoso) + Na 2 O 2 (acuoso) + 3HgO(s)
→ Sb 2 S 5 + Na 2 S + Sb 2 S 3 + O 2 + 3Hg
Todos los elementos, excepto el oxígeno, formaron un único complejo no identificable y térmicamente inestable.
PRUEBA 3. Se añadió cloruro de mercurio a una parte de la kermesita (?) en un tubo de ensayo y se aplicó calor hasta que la secuencia de cambios de color pareció completarse. Tras dejarla enfriar hasta que cambió de aspecto, se recalentó para eliminar el agua restante y se calentó en un matraz de fondo redondo de 0,5 l con termómetro, comprobando su estabilidad térmica. La trituración del producto resultante sirvió para confirmar su consistencia y solidez.
Observaciones e interpretación.
Se formó una solución transparente de color rosa cremoso, que al calentarse se tornó marrón oscuro y luego gris. Al enfriarse, se tornó de un amarillo grisáceo claro con un precipitado gris. Al deshidratarse, apareció una concreción gris con una superficie blanca pulverulenta, pero casi toda esta se vaporizó, dejando un blanco cremoso.
22
Recubrimiento sobre toda la superficie interna del matraz, quedando solo unos pequeños grumos cristalinos en el fondo. La trituración produjo un polvo uniforme de color gris parduzco. El polvo blanco cremoso sugiere la presencia de mercurio (finamente dividido), trióxido de antimonio y óxido mercúrico, como parece confirmar su facilidad para vaporizarse. Los grumos restantes probablemente contienen un complejo de sulfuros, y la apariencia del producto triturado respalda esta hipótesis, así como la suposición de que, para esta etapa, todos los iones cloruro se habían emitido como gas cloro. Sin embargo, los sulfuros estables se obtienen fácilmente combinando cinabrio u óxido mercúrico con óxidos o sulfuros de antimonio. No producen óxidos mixtos estables al calentarlos, a menos que, quizás, se calienten en atmósfera de oxígeno o durante mucho más tiempo del habitual dadas las limitaciones de tiempo en un laboratorio moderno.
PRUEBA 4. Se aplicó una capa de pentóxido de antimonio humedecido (<1 g) a una malla de soporte de alambre de hierro y se cubrió con ~1 g de óxido de mercurio (en forma de partículas amarillas). Esta capa se calentó, primero suavemente y luego con más intensidad, en un tramo de tubo de combustión, hasta que el ciclo de cambios pareció completarse. El producto resultante se raspó del alambre y del interior del tubo, se trituró con cristales de hidróxido de sodio y se volvió a colocar, sin soporte, en el tubo. Se calentó con intensidad hasta que se desarrolló una reacción exotérmica y luego se volvió a calentar para observar el producto deshidratado.
Observaciones e interpretación.
La mezcla estratificada se tornó anaranjada y luego a rojo oscuro al calentarse intensamente. Se produjo vaporización, que cesó rápidamente al enfriarse. Pareció solidificarse como un producto marrón anaranjado, pero recuperó su color rojo al recalentarlo. Sin embargo, al añadir cloruro de sodio, primero se volvió negra y húmeda, y luego burbujeó como carbonato de potasio al calentarse. Finalmente, se obtuvo un producto abigarrado de gris claro, azul, verde y amarillo, con vitrificación en el punto de contacto con el tubo de vidrio.
En esencia, las reacciones indican la producción de sal de Schlippe (deshidratada) o tioantimoniato de sodio, que forma cristales tetraédricos amarillos. Estos se verían verdes o azules al mezclarse íntimamente con el mercurio y el antimonio grises. La reacción inicial sería:
2HgO → 2Hg + O 2 (reacción incompleta)
calentada en
presencia de antimonio
seguido de:- 6NaOH + Sb2S3 → 3Na2S + Sb2O3 + 3H2O ( v )
Luego, al recalentar:
Sb 2 S 3 + 3Na 2 S + HgO + Sb 2 O 3 → 2Na 3 SbS 4 + Hg + 3O 2
Difracción de rayos X
Esto se utiliza para distinguir los planos cristalinos que comprenden átomos de un elemento de los de otro. Los rayos X no tienen carga, al ser ondas electromagnéticas, pero interactúan con los electrones que rodean los núcleos atómicos. Dado que el número y la distribución de electrones difieren en los átomos de distintos elementos, reflejan los rayos X de forma distinta. El resultado es que una serie de planos de reflexión para cada elemento involucrado, al ser expuestos a la incidencia de rayos X, reflejan los rayos en diferentes ángulos, denominados ángulos de dispersión. Esto produce un conjunto completo de picos en la intensidad de los rayos reflejados, relacionado con dichos ángulos de dispersión, para cada uno de los elementos de un compuesto.
Los rayos X se generan mediante interacciones entre electrones. En 1913, Henry Moseley investigó la producción de rayos X bombardeando muestras de diferentes elementos con electrones y midiendo la energía de los rayos emitidos mediante el registro de su dispersión desde un único cristal de ferrocianuro de potasio. Einstein ya había calculado la relación entre la energía de una onda y su frecuencia, que se expresa mediante su ecuación E = hf, donde h es la constante de Planck. Así, Moseley pudo calcular la frecuencia, f, de sus rayos X a partir de su energía, E. Encontró que la frecuencia estaba relacionada con el número atómico, Z, del elemento bombardeado mediante:
f = a(Z - b) 2
donde a y b son constantes.
Ahora bien, como la frecuencia de una onda está relacionada con su longitud de onda, l , por :- c = f l , siendo c la velocidad de la luz, Moseley pudo comprobar el espaciamiento entre los planos atómicos de su cristal dispersor utilizando la ecuación de Bragg :-
n l = 2d sen q (véase el Apéndice D). Por supuesto, tuvo que usar esta ecuación para derivar la longitud de onda y, por consiguiente, la energía de los rayos, pero el ajuste de la posición del cristal proporcionó picos de intensidad relacionados con los diferentes ángulos de dispersión (2 q ), lo que le permitió comprobar la consistencia de la relación entre sus valores de d y E en todo el rango de intensidad.
Maximizar el número de planos cristalinos disponibles en un ángulo dado con respecto a los rayos X incidentes maximiza la intensidad de los rayos reflejados para ángulos en los que están en fase. Moler la muestra de prueba cristalina hasta obtener un polvo fino maximiza el número de planos cristalinos en todos los ángulos. Al rotar lentamente una muestra finamente pulverizada del elemento/compuesto en un haz de rayos X que emerge desde una dirección fija, se presenta un gran número de planos cristalinos a dichos rayos. Este es el principio detrás de la cámara de rayos X en polvo Debye-Scherrer, que produce un conjunto de líneas en un negativo que representan los picos de intensidad de los rayos reflejados. El proceso se computarizó posteriormente para generar un gráfico de los recuentos de rayos X que comprenden los picos frente a los ángulos de dispersión.
Un conjunto de picos de intensidad presenta un patrón característico de una estructura cristalina particular, pero esto no implica que la estructura en sí sea fácilmente identificable. Esto se debe a que la posición de los átomos en un cristal se representa con mucha mayor precisión mediante la posición de sus diminutos núcleos que mediante la dispersión de sus capas electrónicas. Son estas posiciones atómicas las que identifican la estructura cristalina (véase 11. Difracción de neutrones). Si bien la intensidad con la que los rayos se reflejan desde los átomos que componen las celdas unitarias de la estructura cristalina es crucial para determinar su composición, el cálculo de la intensidad apropiada para una estructura dada es un proceso mucho más complejo que el del espaciamiento entre planos. Viene dado por:
Yo 0 = K 2 CS 0 2
S 0 se denomina amplitud de la estructura observada, una medida de la amplitud de las ondas reflejadas por unidad de celda.
I 0 es la intensidad observada por unidad de celda de rayos X reflejados.
K es un factor de escala relacionado con S 0 .
C es un factor que depende de las características celulares y de las condiciones experimentales.
Como era de esperar, es mucho más fácil comparar la intensidad de los rayos X reflejados para una celda unitaria conocida, utilizando datos derivados de un experimento previo con muestras fiables y puras analizadas repetidamente para obtener una referencia estándar, que empezar de cero y obtener una imagen de la estructura simplemente analizando una muestra de prueba e intentando estimar K y C. Sin embargo, conviene abordar el problema como si las condiciones ambientales, y por ende C, fueran constantes durante un período razonable de exposición a rayos X, por ejemplo, dos horas, de modo que la relación entre la intensidad y la amplitud de la estructura pueda considerarse constante para un experimento dado. De esta manera, al menos, se pueden realizar comparaciones significativas entre los picos de intensidad de la muestra de prueba y los del estándar. Esto se debe a que, una vez asociados los picos con planos de reflexión específicos, las proporciones de las intensidades de los picos entre sí son constantes para cualquier estructura en particular; es decir, no es necesario calcular sus valores absolutos individuales según la fórmula. Las intensidades relativas de los picos identificados para una muestra de prueba pueden compararse con las del estándar y extraer conclusiones. Lamentablemente, no siempre hay disponible un estándar confiable, particularmente en el caso de un compuesto raro, y esa fue la situación en la que me encontré con respecto al piroantimoniato de mercurio.
Difracción de neutrones
1. La interacción nuclear de corto alcance del neutrón con el núcleo atómico. Esto es similar para diferentes elementos, ya que las fuertes resonancias asociadas al proceso de dispersión impiden cualquier variación regular de las amplitudes de las ondas de dispersión nuclear con el número atómico.
2. La interacción del momento magnético del neutrón con los momentos magnéticos de espín y orbital del átomo. La amplitud de la interacción varía con el tamaño y la orientación del momento magnético atómico, y la intensidad de la dispersión depende del ángulo de espín de los electrones magnéticos en el átomo.
La distribución angular de los neutrones dispersos se mide al determinar la estructura de muchos materiales. Se pueden examinar tanto muestras policristalinas como monocristalinas, pero las técnicas monocristalinas proporcionan una resolución mucho mejor de los picos de difracción. Sin embargo, una aplicación significativa en cristalografía química es la determinación de la estructura de cristales compuestos que contienen átomos tanto pesados como ligeros (y la relación de las masas atómicas relativas de Hg a O ~ = 25:2 y de Sb a O ~ = 15:2). El análisis de cristales mediante el interferómetro de neutrones (inventado en 1974) se facilita mediante el crecimiento de cristales enormes, esencialmente perfectos (de hasta 10 cm). Afortunadamente, los informes de los alquimistas sugieren que el mercurio rojo tiende a imitar a la kermesita, un mineral oxisulfuro de antimonio, en su propensión a la cristalización.
Masas involucradas en la preparación de Hg 2 Sb 2 O 7
[Error = 0,02 g en todo el texto a menos que se especifique lo contrario]
Reactivos: - Relación de masa molar requerida de óxido:ácido = 434:360 = 1,206:1
Masa del vaso de precipitados 1 + H 4 Sb 2 O 7 = 65,34 g -
Masa del vaso 1 = 54,86 g
= Masa de H 4 Sb 2 O 7 = 10,48 g ? 0,03 g
Masa del vaso de precipitados 2 + HgO = 19,33 g -
Masa del vaso de precipitados 2 = 7,14 g
=Masa de HgO = 12,19 g ? 0,03 g
Las masas medidas tienen una relación de óxido a ácido de 1,163:1
Masa del tubo de ebullición 1 + reactivos = 68,00 g
-
Masa del tubo de ebullición 1 = 45,33 g
= Masa de reactivos = 22,67 g ?0,03 g
Producto : Relación de masa molar de los reactivos con el óxido doble deseado = 794:758 = 1,048:1
Por lo tanto, la masa esperada de Hg 2 Sb 2 O 7 = 22,67 g / 1,048 = 21,63 g
(ignorando por ahora las discrepancias entre las relaciones de masa requeridas y medidas).
Masa final del tubo de ebullición 2 + producto,
después de calentar con oxígeno y expulsar el vapor del tubo = 63,95 g -
Masa del tubo de ebullición = 43,74 g
= Masa de Hg 2 Sb 2 O 7 = 20,21 g
(Error en estos últimos valores es ? 0,05 g)
La cantidad de agua perdida por evaporación del agua generada durante la reacción puede calcularse a partir de las masas de los reactivos y el producto esperado, y es de 1,04 g. La diferencia restante de 1,42 g entre la masa esperada del producto y la encontrada es fácilmente atribuible a la pérdida de Hg a través del tubo de salida de oxígeno, junto con cualquier nitrato restante como impureza del proceso de producción de HgO. Asimismo, también se debería a la discrepancia en las proporciones de masa requeridas y medidas de los reactivos, siendo el ácido el componente determinante (o limitante) y el HgO sobrante sublimando, con Hg, como una "escarcha" en el interior del tubo de ebullición. Tiene algo de la naturaleza del nitrato, pero es pulverulento en lugar de tener la apariencia áspera y acicular de este último.
PROCESAMIENTO POSTERIOR DEL PIROANTIMONATO Y DE LAS MASAS ENCONTRADAS, JUNTO CON UNA INTERPRETACIÓN.
Calentando repetidamente el producto bajo oxígeno y devolviéndole cualquier sublimado adicional, calentándolo también en el tubo de ebullición parcialmente evacuado sobre una vela y durante la noche, se acercó gradualmente a una condición en la que era térmicamente "semiestable". Habiendo repetido este procedimiento en varias ocasiones en las que he llevado a cabo este experimento, con variaciones, puedo afirmar que esto nunca toma menos de 3 semanas.
Luego, tras un largo periodo calentándolo con una vela, gradualmente pasó de un color ocre amarillento a un blanco crema. Calentado de nuevo con un mechero Bunsen, se volvió blanco como la tiza. color. Había mucho sublimante y esto fue recogido.
Masa del sublimado de Hg 2 Sb 2 O 7 + placa de Petri = 13,090 g
_
Masa de la placa de Petri = 6,953 g
Masa del sublimado = 6,137 g ? 0,03 g
Masa del residuo + tubo de ebullición = 63,751 g
_
Masa del tubo de ebullición = 52,369 g
Masa del residuo = 11,382 g ? 0,03 g
La interpretación de los escaneos de rayos X de mis muestras de óxido, los ajustes en mi enfoque experimental y los resultados finales de los experimentos.
Si no está familiarizado con los principios de la cristalografía de rayos X, consulte el APÉNDICE D. CRISTALOGRAFÍA BÁSICA . Aquí observará que la última ecuación de la sección «Ley de los Índices Racionales» es:
h2 / a2 + k2 / b2 + l2 / c2 = 1 / d2
Lo más importante a destacar en este punto es que el Dr. Sleight identificó el piroantimoniato mercúrico como un compuesto con una estructura cúbica de pirocloro . Como las longitudes a, b y c se identifican con los ejes ortogonales de la celda unitaria, que en este caso es un cubo, a = b = c. Por lo tanto, la ecuación se simplifica a:
h2 / a2 + k2 / a2 + l2 / a2 = 1 / d2
(h2 + k2 + l2 ) / a2 = 1/ d2
En este punto, consulte la ecuación para las reflexiones de primer orden, que aparece en la sección 'Rayos X y los átomos en una red cristalina':
sen 2 q B = ( l 2 /4)(1/d 2 )
A continuación, sustituya el valor derivado previamente para 1/d 2 en esta ecuación, para obtener:
sen 2 q B = ( l 2 /4)(h 2 + k 2 + l 2 )/a 2
Esta es la ecuación de la que se derivan los valores de los ángulos de Bragg, q B . La longitud al cuadrado h 2 + k 2 + l 2 es el cuadrado de la hipotenusa para el equivalente tridimensional del teorema de Pitágoras. Es igual a S 2 , siendo S el factor de estructura .
El Dr. Sleight determinó que la estructura del piroantimoniato mercúrico era cúbica centrada en las caras,
con un borde de celda a = 10,349 Ångströms. (El Ångström = 1 × 10⁻¹ de un metro). Ahora consulte la fórmula de Bragg para una estructura cristalina cúbica:
sen 2 q B = ( l 2 /4)(h 2 + k 2 + l 2 )/a 2
Sustituyendo «a» y usando l = 1,54 Ångströms (elevado a 3 sfs), se obtiene un valor de l /a de 0,1488066, denotado «r» en las siguientes listas. Los ángulos de Bragg y de dispersión son, según mis cálculos:
hkl sin q B = [S/2]r q B q S = 2 q B (a 3 sfs)
1 1 1 (3/4) r 7,40 14,8
3 1 1 (11/4) r 14,29 28,6
2 2 2 (3) r 14,94 29,9
4 0 0 2r 17.31 34.6
3 3 1 (19/4) r 18,92 37,9
5 1 1 (27/4) r 22,74 45,5
4 4 0 (8) r 24,89 49,8
5 3 1 (35/4) r 26,12 52,2
6 2 2 (11) r 29,57 59,2
4 4 4 (12) r 31.03 62.1
7 1 1 (51/4) r 32,10 64,2
5 5 3 (59/3) r 34,86 69,7
35
Intensidades observadas por el Dr. Sleight I obs . para la muestra de Hg 2 Nb 2 O 7 , en lugar de Hg 2 Sb 2 O 7 (ambas con una estructura de pirocloro 'con el mismo parámetro posicional') expresadas como proporciones del pico más pequeño, reflejado desde los planos {444}.
Todos estos picos están por encima de 1.000 cps.
hkl obs
{222} 10.26
{400} 3.51
{440} 4.06
{622} 3.94
{444} 1.00
Datos equivalentes (I obs ) para escaneos obtenidos con datos de mis propias muestras. Todos los picos utilizados para este propósito tenían +/- 1 de los ángulos obtenidos utilizando el valor de 10,349 Å del Dr. Sleight para los planos reticulares relevantes.
Escanear 15 16 17 19 20 21
hk 1 Hg 2 Sb 2 O 7 -> |Hg 2 Sb 2 O 7 + Hg 2 Sb 2 O 6
{222} 3,40 2,02 2,40 4,64 6,40 5,51
{400} - 1,42 1,43 1,77 2,44 2,36
{440} 1,62 1,22 1,14 2,03 2,75 2,37
{622} - 1,12 1,31 2,23 2,60 2,10
{444} 1.00 1.00 1.00 1.00 1.00 1.00
6. Conclusiones extraídas de las comparaciones de mis muestras con las descritas en el informe del Dr. Sleight.
Como el sublimado del Hg 2 Sb 2 O 7 tiene toda la apariencia de ser HgO impuro y tiene una masa = 0,503 de la masa de HgO añadido originalmente, se podría suponer que el residuo era HgSb 2 O 6 . Ahora, los escaneos de difracción 17 a 21 demuestran la compatibilidad entre los ángulos de dispersión para el residuo y los calculados utilizando los datos del Dr. Sleight para Hg 2 Sb 2 O 7 . La masa del residuo y la calculada para el producto de la reacción principal están en la relación 0,526:1, lo que sugiere que, dentro de un error permisible de ? 0,5 g, la mitad del Hg 2 Sb 2 O 7 producido se ha perdido posteriormente, pero el residuo sigue siendo el piroantimoniato. Sin embargo, el escaneo 22 confirma la primera impresión dada por el sublimado; Se trata predominantemente de HgO y, por lo tanto, el residuo no puede ser piroantimoniato puro. La experiencia ha demostrado que los compuestos de antimonio, al igual que este elemento, son menos volátiles que los compuestos de mercurio. La alta estabilidad térmica del residuo en su forma de color crema, que se observa que se convierte eventualmente en una sustancia marrón rojiza al calentarse intensamente, sugiere que el Dr. Sleight, o mejor dicho, sus asistentes, diagnosticaron erróneamente este último compuesto. Consideró que «en muestras aparentemente ligeramente deficientes en mercurio y oxígeno, el tamaño de la celda disminuyó», por lo que, dado que la estructura FCC y la dimensión del borde de la celda unitaria que cita parecen aplicarse al residuo, no puede ser un compuesto puro con la fórmula Hg₂Sb₂O₄ .
Especulando que el residuo es una combinación de Hg2Sb2O7 y HgSb2O6 en la relación molar 1:1, la relación de masa de HgO al óxido restante es la de 3HgO a 2Sb2O5 o 650 : 647 . Esto es 1: 1 dentro de los márgenes de error involucrados. Agregue la mitad de la masa del residuo (5,69 g) a la del sublimado (6,14 g) y la suma (11,83 g) está dentro de 0,5 g de la masa de HgO introducida originalmente (12,19 g). La pérdida equivalente de Sb2O5 se ve como 9,44 g - 5,69 g = 3,75 g. Dada la volatilidad relativa de los metales, la relación de las pérdidas de óxido sugeridas aquí, 1,64:1, ciertamente está en línea con las expectativas. Una estructura FCC con la fórmula compuesta Hg 3 Sb 4 O 13 , que comprende 80 átomos por celda unitaria, es decir, con Z = 4, y dispuesta como redes alternas de octaedros de SbO 6 más cadenas de HgO y octaedros de SbO 6 más cadenas de Hg en simetría cuádruple parecería ajustarse a la descripción. Cualquier otra cosa probablemente sería una mezcla, al menos en parte, de modo que tendría una menor estabilidad térmica y exhibiría muchos más picos en el escaneo de difracción de rayos X. Por supuesto, solo el análisis espectroscópico de masas podría confirmar las razones de masa de los elementos presentes, pero el análisis de difracción al menos apunta a una alternativa creíble a la interpretación del Dr. Sleight de las muestras de Hg 2 Sb 2 O 7 de diferente color con sus purezas variables.
